 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某元素基态原子,有量子数n=4、1=0、m=0的一个电子,有n=3、i=2的5个电子,该原子的价层电子构型为(
),位于周期表第()周期、第()族、元素名称(),元素符号()。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
),位于周期表第()周期、第()族、元素名称(),元素符号()。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某元素基态原子,有量子数n=4、1=0、m=0的一个电子,有…”相关的问题
更多“某元素基态原子,有量子数n=4、1=0、m=0的一个电子,有…”相关的问题
基态Ni原子可能的电子组态为:(1)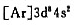 ,(2)
,(2)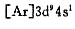 。由光谱实验确定其能量最低的光谱支项为3F4,试判断它是哪种组态。
。由光谱实验确定其能量最低的光谱支项为3F4,试判断它是哪种组态。
一氧化氮(NO)分子被美国《科学》杂志命名为1992年明星分子。在无机化学和生物无机化学中,NO是已得到深入研究的分子之一。
(1)写出基态的价电子组态,并回答下列问题:
(a)N原子和O原子间形成什么形式的化学键?
(b)键级多少?
(c)按原子共价半径估算N-O间的键长,并和实验测定值115pm比较。
(d)分子第一电离能比N2是高还是低?说明原因。比O2又如何?
(e)NO+键级是多少?估计其键长。
(D)NO+的伸缩振动波数比NO是大还是小?估计其数值.
(2)若忽略电子的轨道运动对磁矩的贡献,计算NO分子的磁矩。
(3)已知NO红外光谱的两个谱带的波数分别为1876.2cm-1和3724.6cm-1,计算第三泛音带的波数。
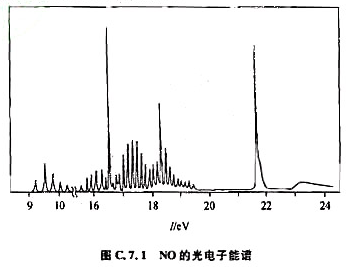
(4)NO紫外光电子能谱(HeⅡ线,40.8eV)的一部分示于图C.7.1中,图中的谱带对应于2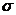 轨道。试解释此能谐分裂为两个谱带(分别对应于3Ⅱ和1Ⅱ态)的原因,并估算从2
轨道。试解释此能谐分裂为两个谱带(分别对应于3Ⅱ和1Ⅱ态)的原因,并估算从2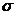 轨道击出的光电子的最大动能。
轨道击出的光电子的最大动能。
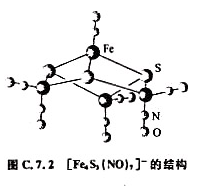
(5)在腌肉时加入NaNO2,产生NO,NO与从蛋白质中解离出来的硫和铁结合生成[Fe4S3(NO)7]-,该离子有抑菌、防腐作用。X射线结构分析表明该离子的结构如图C.7.2所示,请指明该离子所属点群。
设粒子处于无限深方势阱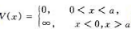 中,粒子波函数为
中,粒子波函数为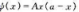 ,A为归一化常数,设粒子处于基态(n=1),
,A为归一化常数,设粒子处于基态(n=1),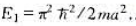 设t=0时刻阱宽突然变为2a,粒子波函数来不及改变,即
设t=0时刻阱宽突然变为2a,粒子波函数来不及改变,即
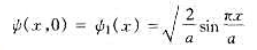
试问:对于加宽了的无限深方势阱

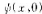 是否还是能量本征态?求测得粒子处于能量本征值
是否还是能量本征态?求测得粒子处于能量本征值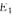 的概率。
的概率。
设a,b,c,d代表不同的元素,说明以下集合A和B之间成立哪一种关系(指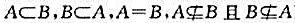 )。
)。
(1)A={{a,b},{c},{d}},B={{a,b},{c}}。
(2)A={{a,b},{b},∅},B={{b}}。
(3)A={x|x∈N∧x2>4},B={x|x∈N∧x>2}。
(4)A={ax+b|x∈R∧a,b∈Z},B={x+y|x,y∈R}。
(5)A={x|x∈R∧x2+x-2=0},B={y|y∈Q∧y2+y-2=0}。
(6)A={x|x∈R∧x2≤2},B={cx|x∈R∧2x3-5x2+4x=1}。