 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
取钢试祥1.00g,溶解于酸中,将其中锰氧化成高链酸盐准确配制成250mL,测得其吸光度为1.00x10-3mol·L-1KMnO4溶液的吸光度的1.5倍.计算钢中锰的百分含量.
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“取钢试祥1.00g,溶解于酸中,将其中锰氧化成高链酸盐准确配…”相关的问题
更多“取钢试祥1.00g,溶解于酸中,将其中锰氧化成高链酸盐准确配…”相关的问题
锰及其他金属元素,称取127.3mg试样溶解在酸中并加入适当掩蔽剂,以防止其他金属离子的干扰。铁和锰分别以Fe(C9H6NO)3(相对分子质量:488.28) 和Mn(C9H6NO)2(相对分子质量:343.23) 的形式沉淀,共得到沉淀867.8mg,同时用去8-羟基喹啉5.276mmol.试分别计算铁和锰的含量。
A.从送检样品中均匀取两个平行试样,每个试祥约重 400~600g
B.称得试样重量,在油光纸上将烟把解开,用毛刷逐片正反两面各轻刷 5~8 次,刷净
C.搜集刷下的砂土,通过分离筛,至筛不下为止
D.将筛下的砂土称重,记录重量计算
间接法测定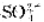 时,称取3.000g试样溶解后,稀释至250.00mL。在25.00ml.试液中加入25.00mL 0.05000mol·L-1BaCl2溶液,过滤BaSO4沉淀后, 滴定剩余Ba²+用去29.15ml.0.02002mol·L-1EDTA。试计算
时,称取3.000g试样溶解后,稀释至250.00mL。在25.00ml.试液中加入25.00mL 0.05000mol·L-1BaCl2溶液,过滤BaSO4沉淀后, 滴定剩余Ba²+用去29.15ml.0.02002mol·L-1EDTA。试计算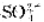 的质量分数, 已知M(
的质量分数, 已知M(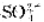 )=96.06g·mol-1.
)=96.06g·mol-1.
mol·L-1EDTA.试计算SO42-的质量分数.
重量分析法用于测定矿石中的磁铁矿(Fe3O4)的含量。称取1.5419g试样,用浓盐酸溶解后,得到Fe2+和Fe3+的混合溶液。加入硝酸将Fe2+氧化至Fe3+,稀释后用氨水将Fe3+沉淀为Fe(OH)3。将沉淀过滤,洗涤和灼烧后得0.8525gFe2O3,计算Fe2O3的质量分数?已知摩尔质量:Fe2O3为159.69g·mol-1Fe3O4为231.55g·mol-1.