 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
反应200℃时标准平衡常数= 0.64,400℃时标准平衡常数=6.0×10-4,据该反应的标准摩尔反应热和NH
反应
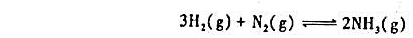
200℃时标准平衡常数 = 0.64,400℃时标准平衡常数
= 0.64,400℃时标准平衡常数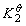 =6.0×10-4,据该反应的标准摩尔反应热
=6.0×10-4,据该反应的标准摩尔反应热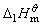 和NH3(g)的标准摩尔生成热
和NH3(g)的标准摩尔生成热 。
。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应
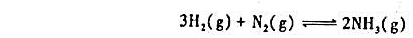
200℃时标准平衡常数 = 0.64,400℃时标准平衡常数
= 0.64,400℃时标准平衡常数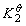 =6.0×10-4,据该反应的标准摩尔反应热
=6.0×10-4,据该反应的标准摩尔反应热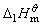 和NH3(g)的标准摩尔生成热
和NH3(g)的标准摩尔生成热 。
。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“反应200℃时标准平衡常数= 0.64,400℃时标准平衡常…”相关的问题
更多“反应200℃时标准平衡常数= 0.64,400℃时标准平衡常…”相关的问题
25℃时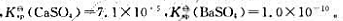 则沉淀转化反应:
则沉淀转化反应: 在25℃时的标准平衡常数
在25℃时的标准平衡常数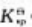 =()。在25℃标准状态下,上述反应方向为()。
=()。在25℃标准状态下,上述反应方向为()。
300K时,合成氨反应: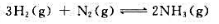 的温度范围内保持不变,计算该可逆反应在600K时的标准平衡常数。
的温度范围内保持不变,计算该可逆反应在600K时的标准平衡常数。
反应 在某温度下达到平衡。
在某温度下达到平衡。
(1)若其他条件不变,加入催化剂是否会引起平衡移动?
(2)若增大任一反应物或生成物的分压,化学平衡向哪一方向移动?
(3)升高温度时标准平衡常数是否发生变化?化学平衡向哪一方向移动?
(4)缩小容器的体积增大压力时,化学平衡向哪一方向移动?标准平衡常数是否发生变化?
已知在1mol·L-1HC 1介质中,Fe(III)/Fe(II) 电对的Eθ=0.70V.
Sn(Ⅳ)/Sn(Ⅱ)电对的Eθ=0.14V.求在此条件下,反应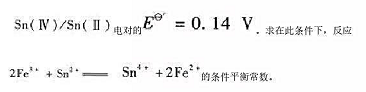 的条件平衡常数。
的条件平衡常数。
已知300K时: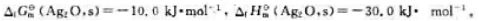
(1)试通过计算说明在300K、标准状态下、Ag2O(s)能否发生如下分解反应:
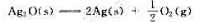
(2)计算在标准状态下Ag2O(s)发生分解反应的最低温度。