 更多“ 测定含铁量实验中,高锰酸钾溶液的质量分数为()。”相关的问题
更多“ 测定含铁量实验中,高锰酸钾溶液的质量分数为()。”相关的问题
第1题
称取褐铁矿试样0.4000g,用HCI溶解后,将Fe3+还原为Fe2+,用K2Cr2O7标准
溶液滴定.若所用K2Cr2O7溶液的体积(以mL为单位)与试样中Fe2O3的质量分数相等.求K2Cr2O7溶液对铁的滴定度.
点击查看答案
第2题
用0.1018mol·L-1 NaOH标准溶液测定某草酸试样的纯度,为避免计算,欲直接用所消相NaOH溶液的体积(单位m)来表示试样中H2C2O4的质量分数(%),问应称取试样多少克?
用0.1018mol·L-1NaOH标准溶液测定某草酸试样的纯度,为避免计算,欲直接用所消相NaOH溶液的体积(单位m)来表示试样中H2C2O4的质量分数(%),问应称取试样多少克?
点击查看答案
第3题
称取含Kl之试样1.000g溶于水.加10mL0.05000mol·L-1KIO3溶液处理,反应后煮沸驱尽所
生成的I2,冷却后,加入过量KI溶液与剩余的KIO3反应.析出I2的需用21.14mL0.1008mol·L-1
点击查看答案
Na2S2O3溶液滴定.计算试样中KI的质量分数.
第4题
有一含酸性组分CO2的混合气体,在常温下取样品气体100mL,经烧碱(NaOH)溶液吸收后,在相同室温和常压下测得剩余气体的体积为99.5mL,试向此混合气体中CO2的物质的量分数为多大?
第5题
重量分析法用于测定矿石中的磁铁矿(Fe3O4)的含量。称取1.5419g试样,用浓盐酸溶解后,得
重量分析法用于测定矿石中的磁铁矿(Fe3O4)的含量。称取1.5419g试样,用浓盐酸溶解后,得到Fe2+和Fe3+的混合溶液。加入硝酸将Fe2+氧化至Fe3+,稀释后用氨水将Fe3+沉淀为Fe(OH)3。将沉淀过滤,洗涤和灼烧后得0.8525gFe2O3,计算Fe2O3的质量分数?已知摩尔质量:Fe2O3为159.69g·mol-1Fe3O4为231.55g·mol-1.
第6题
用碘量法测定铬铁矿中铬的含量时,若溶液中Fe(III) 的浓度为0.10mol·L-1, Fe(II) 的浓
用碘量法测定铬铁矿中铬的含量时,若溶液中Fe(III) 的浓度为0.10mol·L-1, Fe(II) 的浓
点击查看答案
度为1.0×10mol·L-5,铁电对的电势是多少?共存的Fe(Ⅲ) 对测定有无干扰?若加入EDTA并使其过量的浓度为0.10mol·L-1,问此条件下, 铁电对的条件电势是多少?Fe(III) 的干扰能否被消除?
第7题
把30.0g乙醇(C2H5OH)溶于50.0g四氯化碳(CCl4)所配成的溶液密度为1.28g·mL-1.试计算:(1)乙醇的质量分数:(2)乙醇的摩尔分数;(3)乙醇的质量摩尔浓度;(4)乙醇的物质的量浓度.
把30.0g乙醇(C2H5OH)溶于50.0g四氯化碳(CCl4)所配成的溶液密度为1.28g·mL-1.试计算:(1)乙醇的质量分数:(2)乙醇的摩尔分数;(3)乙醇的质量摩尔浓度;(4)乙醇的物质的量浓度.
点击查看答案
第8题
某试样含Cl-的质量分数的平均值的置信区间为36.45%士0.10%(置信度为90%),对此结果应理解为().
A.有90%的测定结果落在36.35%~36.55%B总体平均值μ落在此区间的概率为90%
B.若再作一次测定,落在此区间的概率为90%
C.在此区间内,包括总体平均值p的把握为90%
第9题
含醋酸0.20(质量分数,下同)的水溶液100kg,用纯乙醚为溶剂作多级逆流萃取,采用溶剂比S/F为1,以使最终萃余相中含醋酸不高于0.02。操作在25℃下进行,试求:最终萃取相的量及组成、最终萃余相的量及组成。
含醋酸0.20(质量分数,下同)的水溶液100kg,用纯乙醚为溶剂作多级逆流萃取,采用溶剂比S/F为1,以使最终萃余相中含醋酸不高于0.02。操作在25℃下进行,试求:最终萃取相的量及组成、最终萃余相的量及组成。
点击查看答案
第11题
测定氯苯中的微量杂质苯、对二氧苯、邻二氧苯时,以甲苯为内标,先用纯物质绘制标准曲线,得如下数
据.试根据这些数据绘制峰高比与质量比之间的关系曲线.
点击查看答案
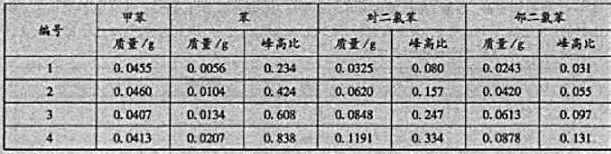
在分析未知试样时,称取氯苯试样5.119g,加入内标0.0421g,测得色谱图,从图上量取各色谱峰的峰高.并求得峰高比如下,求试样中各杂质的质量分数:苯与甲苯峰高之比值=0.341,对二氧苯与甲苯峰高之比值=0.298,邻二氧苯与甲苯峰高之比值二0.042.


 如果结果不匹配,请
如果结果不匹配,请 
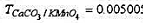 ,求此高锰酸钾溶液的浓度及它对铁的滴定度.
,求此高锰酸钾溶液的浓度及它对铁的滴定度.
















