题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
当氢原子从某初始状态跃迁到激发能(从基态到激发态所需的能量)为△E=10.19eV的状态时,发射出光子的波长是λ=4
当氢原子从某初始状态跃迁到激发能(从基态到激发态所需的能量)为△E=10.19eV的状态时,发射出光子的波长是λ=486nm,试求该初始状态的能量和主量子数。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
当氢原子从某初始状态跃迁到激发能(从基态到激发态所需的能量)为△E=10.19eV的状态时,发射出光子的波长是λ=486nm,试求该初始状态的能量和主量子数。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“当氢原子从某初始状态跃迁到激发能(从基态到激发态所需的能量)…”相关的问题
更多“当氢原子从某初始状态跃迁到激发能(从基态到激发态所需的能量)…”相关的问题
A.1种
B.2种
C.3种
D.4种
A.氢原子的核外电子从低能级跃迁到高能级时,吸收光子,电子的轨道半径增大
B.23892U→23490Th+42He是核裂変方程,当铀块体积大于临界体积时,才能发生链式反应
C.从金属表面逸出的光电子的最大初动能与照射光的强度无关,与照射光的频率成正比
D.α射线是高速运动的氦原子核,能够穿透几厘米厚的铅板
A.基态原子
B.激发态
C.低能态或基态
A.电子轨道半径减小,动能要增大
B.氢原子跃迁时,可发出连续不断的光谱线
C.由n=4跃迁到n=1时放出光子的频率最小
D.金属钾的逸出功为2.21 eV,能使金属钾发生光电效应的光谱线有4条
A.原子核内的一个中子转化成一个质子和一个电子,这种转化产生的电子发射到核外,就是β粒子,这就是β衰变
B.氡222的半衰期是3.8天,镭226的半衰期是1 620年,所以一个确定的氡222核一定比一个确定的镭226核先衰变
C.按照玻尔理论,氢原子核外电子从半径较小的轨道跃迁到半径较大的轨道时,电势能增大,电子的动能减小,原子的总能量减小
D.原子核越大,它的结合能越高,原子核能级越稳定
已知电子沿着团环运动(如图C.3.1)的势能函数V为:
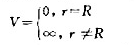
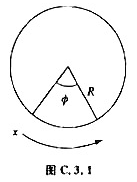
r是电子到四环中心的距离。其Schrodinger方程为:
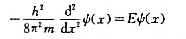
将变数x改成与角度有关的函数,x=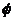 R,解此方程可得波函数
R,解此方程可得波函数
ψn和相应能量En的表达式如下:

(1)以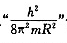 作能量单位,作图示出能级的高低及能简并情况。
作能量单位,作图示出能级的高低及能简并情况。
(2)画出吡啶(C5H5N)和吡咯(C4H4NH)的价键结构式。将环中的π电子运动情况近似地看作如图C.3.1所示的状态,说明环中π键电子的数目,以及它们的LUMO和HOMO。将电子从HOMO跃迁到LUMO,哪一种化合物所需的光的波长短些?
(3)在吡啶盐酸盐(C5H5NH+•Cl-)中。正离子中π键电子数是多少?为什么中性的吡咯C4H4NH能稳定存在,而中性的C5H5NH不稳定?
(4)联系讨论单环共轭多烯体系4m+2规则的本质。
根据氢原子的半经典理论,氢原子处在正常状态(基态)时,它的电子在半径为a=0.52×10-8cm的轨道(叫做玻尔轨道)上作匀速圆周运动,速率为ν=2.2×108cm/s,已知电子电荷为e=1.6×10-19C。试求